Химическая энергия, химическое горение
До сих пор мы давали общее описание некоторых наиболее распространенных молекул. Условия нашей среды на Земле таковы, что молекулы непрерывно разлагаются и снова образуются. Если бы температура Земли была значительно выше, например, если бы она достигала температуры поверхности Солнца, то молекулы никогда не образовывались бы из-за слишком сильного теплового возбуждения: атомы не могли бы оставаться друг возле друга. Если бы ее температура была гораздо ниже, молекулы соединились бы, образуя твердые тела и кристаллы, и никакие изменения не происходили бы. Температура на Земле такова, что имеется иногда достаточно энергии для разрушения некоторых молекул, однако количество этой энергии не слишком велико, и поэтому большинство соединений может существовать в течение некоторого времени. Создание и разрушение молекул характеризует окружающую нас среду, сообщая ей постоянные изменения, которые мы видим, и создавая тем самым возможность жизни.
Одно из важнейших следствий образования молекул состоит в высвобождении энергии. Этот процесс особенно ясно виден при сжигании угля или других веществ. Горение любого типа связано с образованием новых молекул, в результате чего выделяется тепловая энергия. Мы должны теперь выяснить более точно, как и почему освобождается энергия при соединении атомов в молекулы. Химическая связь представляет энергию в таком смысле: для разрыва связи требуется некоторое количество энергии, следовательно, то же ее количество высвобождается при образовании связи. В качестве простейшего примера связи, отличной от химической, рассмотрим магнит, удерживающий кусок железа силой магнитного притяжения (рис. 38).
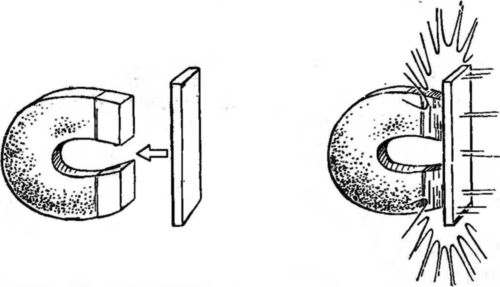
Рис. 38. Когда железка ударяется о магнит, энергия магнитного притяжения превращается в тепло и звук.
Чтобы удалить железо от магнита, требуется некоторая энергия. Когда железо возвращается к магниту, то же количество энергии выигрывается. Это количество энергии создается притяжением к магниту. При удалении железа от магнита энергию поставляют наши мышцы. Где появляется энергия, производимая при возвращении железа к магниту? Часть ее выделяется в виде звука, когда железо ударяется о магнит, часть — в виде тепла, так как при ударе железа о магнит оно нагревается. Эту энергию можно использовать и для выполнения механической работы: если мы прикрепим к железу веревку, перекинутую через блок, а на другой ее конец подвесим грузик, то увидим, что притяжение к магниту будет совершать работу (рис. 39).
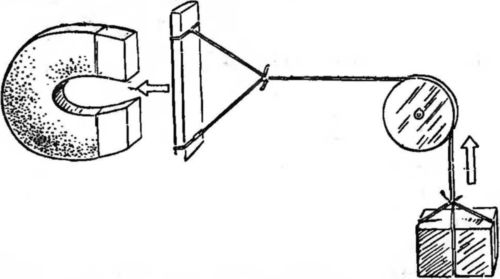
Рис. 39. При таком расположении магнита и пластинки энергия притяжения используется для подъема груза.
Аналогичный обмен энергией происходит и в случае химической связи. Нужно затратить энергию, чтобы разделить молекулу на атомы, и энергия выделяется, когда атомы образуют молекулу. Полученная энергия принимает различные формы. Например, она может проявиться в виде колебаний. Когда атомы соединяются, получившаяся молекула начинает колебаться в результате сильного столкновения атомов. Может получиться и энергия поступательного движения: когда атомы сталкиваются и сливаются, их энергия передается соседним молекулам, скорость которых увеличивается. Вообще, когда бы атомы ни образовали молекулу, энергия освобождается и обычно проявляется в форме движения, что эквивалентно теплу.
Есть некоторые особые случаи, когда энергия связи не превращается в тепло. Это аналогично тому, что притягиваемый к магниту кусок железа производит полезную работу. Некоторые химические реакции присоединения могут происходить таким образом, что энергия, выигранная при образовании молекул, передается молекулам другого рода и переводит их в состояние с большим содержанием энергии. Тогда энергия образования молекулы запасается в другой молекуле вместо того, чтобы растрачиваться в виде тепла. Этот случай важен для поддержания жизни.
Одни химические связи прочны, другие — слабы, рыхлы. Когда образуются прочные связи, освобождается больше энергии. В общем случае связи типа «затычка и дыра» прочнее связей типа «электронные близнецы». Атом водорода труднее оторвать от молекулы воды, чем от молекулы метана.
Рассмотрим более подробно хорошо известный химический процесс, процесс горения угля. Что при этом происходит? Углерод угля и кислород воздуха образуют углекислый газ — двуокись углерода. Кусок угля — это совокупность атомов углерода, расположенных в правильном порядке, кристалл углерода. Кислород воздуха состоит не из отдельных атомов, он существует в виде молекул кислорода, состоящих из двух атомов со связью типа «электронные близнецы». Поэтому химическая реакция горения угля имеет вид C + O = CO2.
Эта реакция должна происходить в два этапа: сначала разрывается связь в молекуле O2, а затем два атома кислорода присоединяются к углероду. Первый этап требует затраты энергии. Он не может происходить при тех энергиях, которые имеются при обычной температуре. В конце концов, уголь может соприкасаться с воздухом без горения. При обычных температурах тепловой энергии недостаточно для расщепления молекулы кислорода на два атома. Но если мы подведем тепло извне от зажженной спички или горящей щепки, то реакция начнется. Надо подвести тепло только для возникновения реакции, так как на втором ее этапе, при образовании СO2, выделяется больше энергии, чем требуется для расщепления O2 (рис. 40).
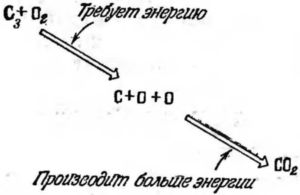
Рис. 40.
Первая связь принадлежит к типу «затычка и дыра», вторая — к типу — «электронные близнецы». Поэтому энергия, необходимая для дальнейшего расщепления O2, поставляется самим процессом горения. Таким образом, при горении угля энергия выделяется в виде тепла, хотя часть энергии, освобождаемой на втором этапе, идет на инициирование дальнейших реакций. Полезное тепло равно избытку энергии, выделяющейся во второй стадии, над энергией, потребной для первой.
Раз начавшись, образование двуокиси углерода продолжается до тех пор, пока не израсходуется весь углерод. Выделяется большое количество тепла; чистый выигрыш энергии составляет 0,67 эв на каждую молекулу образовавшейся двуокиси углерода. Нагревание столь сильно, что атомы и молекулы начинают испускать свет. Пламя, которое мы видим при горении угля, состоит из молекул СO2 и атомов углерода, выброшенных в результате сильного нагрева и испускающих характеристическое излучение. Поэтому пламя не вид вещества, как некогда полагали; это накаленная материя, полученная в химической реакции, в которой выделяется очень много энергии.
Горение угля — это простейшая форма выделения химической энергии. Аналогичный процесс происходит и при горении метана или других углеводородов. И здесь требуется начальное тепло, чтобы расщепить не только молекулы O2, но и молекулы угле водорода. После этого углерод соединяется с кислородом и дает двуокись углерода, а водород соединяется с кислородом и дает воду. Химическая реакция горения метана показана на рис. 41.
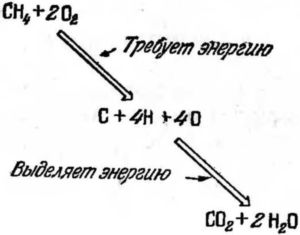
Рис. 41.
Так как в СН4 и O2 связи принадлежат к типу «электронных близнецов», а в СO2, Н2O — к типу «затычка и дыра», чистый выигрыш энергии в этой реакции очень велик. Поэтому метан и другие углеводороды дают сильное пламя и много тепла. Однако в отличие от горения угля, получается не только СO2, но и вода. В пламени содержится вместе с раскаленным СO2 водяной пар. Если подержать холодный кусок стекла в пламени свечи или горящего дерева, то мы увидим на стекле конденсированный водяной пар, которого не получится в пламени чистого угля.
Таким же образом любая молекула, состоящая из углерода, водорода и кислорода, может гореть, т. е. превращаться в углекислый газ и водяной пар, соединяясь с кислородом воздуха. Такие молекулы, как молекулы спирта или сахара, нуждаются в меньшем количестве кислорода для горения, так как в них самих содержится известное количество кислорода.
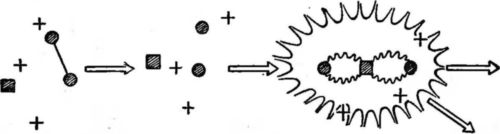
Рис. 42. Горение углерода. Слева мы видим один атом углерода (квадратик), одну молекулу кислорода (два кружка, соединенные связью типа «электронные близнецы») и три другие молекулы, символизированные крестиками. В середине тепловое движение молекулы «крестика» разорвало связь в молекуле кислорода. Справа углерод и два кислородных атома соединились в молекулу СО2. Освободившаяся при этом энергия частично переходит в тепловую энергию молекул «крестиков», частично в энергию колебаний молекулы СО2, что показано «ореолом».
Химические реакции, производящие энергию, всегда должны начинаться с превращения молекул со слабыми связями в молекулы с прочными связями. Разница в энергиях сильной и слабой связи высвобождается. СO2 и вода — это молекулы, с прочными связями; то же относится и к большинству молекул, в которых атомы связаны с кислородом. Однако молекулы, содержащие углерод и водород, связаны слабо, они легко разрушаются и рекомбинируют, могут образовывать длинные цепи и способны собираться в сложные структуры. Если их слабые связи превращаются в сильные связи с кислородом в результате какого-либо сложного процесса, то выделяется энергия. Благодаря этим свойствам они играют важную роль в живой материи.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОК