Молекулы
Рассмотрим несколько специальных примеров. Среди многих способов, которыми соединяются атомы друг с другом, можно выделить связи двух важнейших типов. Один из них — связь типа «электронные близнецы», другой — типа «затычка и дыра»[39]. Характерный пример связи первого типа — связь в самой простой молекуле — молекуле водорода Н2, состоящей всего из двух атомов водорода. Здесь две электронные картины, по одной от каждого атома, сливаются в одну новую картину, в результате чего сами атомы соединяются (см. рис. 28). Это слияние как будто противоречит принципу Паули, согласно которому каждую данную конфигурацию может принять только один электрон. На самом же деле противоречия нет; электрон обладает еще одним интересным свойством, о котором мы упомянем здесь только мимоходом: он вращается вокруг собственной оси. Это вращение называется электронным спином. Далее, здесь возможны только два вида вращения — вправо и влево вокруг данной оси. Поэтому каждую электронную картину надо считать дважды, потому что ее может принимать электрон, вращающийся как в одну, так и в другую сторону. Следовательно, два электрона могут принимать одну и ту же конфигурацию, только если они вращаются в противоположных направлениях. Вот почему электронный спин совместно с принципом Паули играет столь важную роль: две и только две электронные конфигурации могут слиться в одну общую. Молекула водорода может состоять только из двух атомов, но не из трех. Химическая связь становится насыщенной при наличии двух электронов на одной орбите.
Характерным примером связи типа «затычка и дыра» служит связь в молекуле воды Н2O, состоящей из одного атома кислорода и двух атомов водорода. Атом кислорода имеет 8 электронов. Но оказывается, что 10 электронов, обращающихся вокруг ядра, образуют очень компактную и округлую совокупность. Элемент неон, имеющий 10 электронов, химически очень неактивен и не образует никаких молекул, но в атоме кислорода до этой компактной конфигурации не хватает двух электронов. Поэтому ансамбль из 8 электронов можно описать как компактную округлую конфигурацию с двумя дырками в ней. Форма дырки определена, она отвечает конфигурации недостающего электрона. В случае кислорода дырки простираются от поверхности конфигурации до ее центра и расположены под прямым углом одна к другой (рис. 29, а).
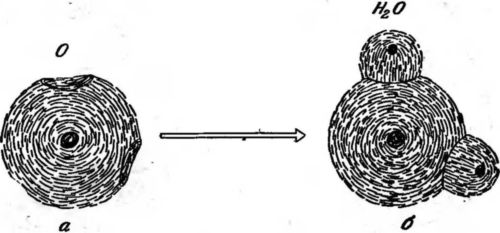
Рис. 29. Атом кислорода (а) и молекула воды (б). электронная конфигурация кислорода имеет две дырки, простирающиеся от ее поверхности до ядра и расположенные под прямым углом. В молекуле воды дырки в кислородном атоме «затыкаются» электронами водорода. Ядра водорода заключены внутри электронных конфигураций водорода (маленькие черные кружки — ядра водорода, большой черный кружок — ядро кислорода).
Теперь мы можем понять строение молекулы воды. Электроны водородных атомов попадают в эти две дырки, атомы водорода служат затычками. Поэтому линии, соединяющие центр атома кислорода с водородными атомами, должны были бы составлять угол 90°. Положительные заряды протонов водородных атомов слегка отталкивают друг друга, что увеличивает этот угол до 108° (рис. 29, б). Это типичная связь типа «затычка и дыра».
Другим интересным примером атома, образующего молекулы, служит атом азота. Он имеет 7 электронов, из которых 4 составляют компактную сферическую конфигурацию вокруг ядра; остальные 3 электрона образуют конфигурации с тремя выступами в трех взаимно перпендикулярных направлениях, например: вверх, вперед и вбок (рис. 30, а).
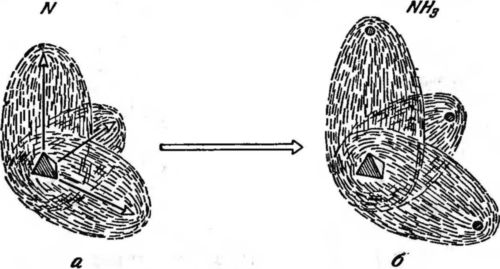
Рис. 30. Атом азота (а) и молекула аммиака (б). В атоме азота мы имеем три электронных выступа, направленных вдоль стрелок под прямыми углами друг к другу. В молекуле аммиака каждый электронный выступ азота сливается с электроном водорода и образует связь типа «электронные близнецы». Густо заштрихованный треугольник — ядро азота; маленькие черные кружки — ядра водорода.
Эта картина позволяет легко понять строение важной молекулы аммиака NH3, в которой три водородных атома дают три связи типа «электронных близнецов», по одной с каждым выступом. Электроны водородных атомов сливаются с электронами выступов, и получается структура, изображенная на рис. 30, б, где ядра водорода сидят на кончиках выступов азота.
Атом углерода особенно приспособлен к образованию молекул. Он имеет шесть электронов, расположенных следующим образом: два электрона находятся близко от ядра и образуют маленькую округлую конфигурацию, остальные четыре могут располагаться симметричным образом, причем каждый дает радиальный выступ, направленный от центра; концы этих выступов расположены по углам правильного тетраэдра (рис. 31, а).
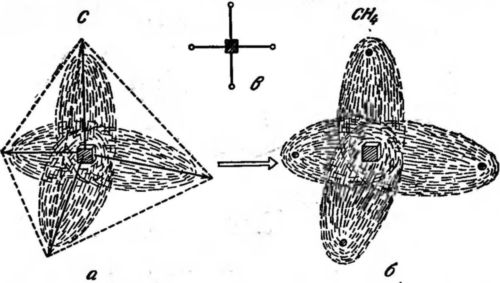
Рис. 31. Атом углерода с четырьмя электронными выступами, направленными по углам правильного тетраэдра (а), молекула метана СН4 (б) и ее схематическое представление (в). Каждый электронный выступ углеродного атома сливается с электроном водорода и образует связь типа «электронные близнецы». Темный квадрат — ядро углерода, маленькие кружки — ядра водорода. Направления связей «близнецы» показаны на (в) отрезками прямых.
Полученная картина позволяет нам понять расположение атомов в молекуле метана СН4, состоящей из одного атома углерода и четырех атомов водорода. Метан является главной составляющей светильного газа. Электроны водородных атомов сливаются с четырьмя выступами в связи типа «близнецы», образуя структуру с ядром углерода в центре и четырьмя протонами по углам тетраэдра (рис. 31, б).
Другая важная молекула, в которую входит углерод, — это двуокись углерода, состоящая из одного атома углерода и двух атомов кислорода. Здесь все четыре выступа слегка изогнуты; два входят в качестве «затычек» в один атом кислорода, остальные два — в другой. В результате получается вытянутая структура из одного углеродного атома и двух кислородных по бокам (рис. 32).
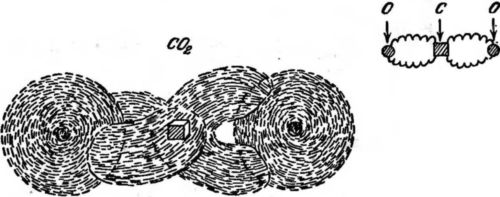
Рис. 32. Молекула двуокиси углерода СO2. Четыре выступа углерода «затыкают» дырки в кислородных атомах. На схеме связи типа «дыра и затычка» показаны волнистыми линиями.
Углеродный атом со своими четырьмя выступами может давать нескончаемый ряд молекул. Это объясняет, почему на Земле так широко распространены соединения углерода и почему они играют столь важную роль в живой материи. Рассмотрим некоторые соединения углерода. Простейшее из них — метан (рис. 33) с одним водородом на каждом выступе.
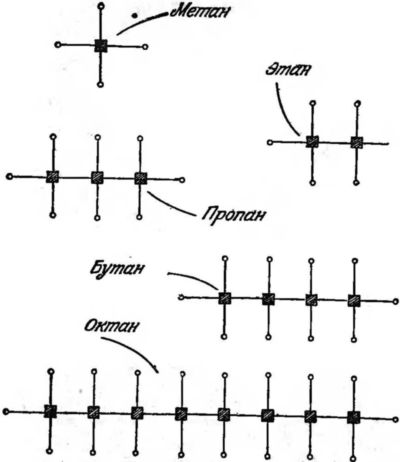
Рис. 33. Схематические изображения молекул углеводородов. Квадратики — атомы углерода, маленькие кружки— атомы водорода, прямые соединительные линии — связи типа «электронные близнецы».
Можно построить и молекулу из двух атомов углерода и шести атомов водорода. Здесь все связи типа «близнецы». Эта молекула называется этаном. Тот же принцип построения можно продолжить (см. рис. 33), и мы получим ряд молекул, называемых углеводородами: пропан с тремя атомами углерода, бутан с четырьмя и т. д. Эта структура, подобная цепи, может иметь любую длину. Короткие молекулы — это газы, более длинные — жидкости и очень длинные — твердые тела. Они служат горючим в виде газа, нефти или парафина, и мы увидим далее, почему они здесь хороши. Углеводородные цепи очень важны и для нашего питания, если они оканчиваются характерной группировкой атомов, называемой карбоксильной группой (рис. 34).
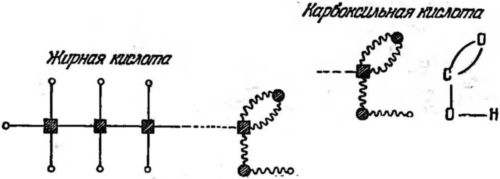
Рис. 34. Схематическое изображение молекул жирных кислот. Длинный углеводород с карбоксильной группой на правом конце. Карбоксильная группа, СООН, состоит из одного атома углерода, двух атомов кислорода и одного атома водорода, соединенных связями типа «дыра и затычка». Квадратики — атомы углерода, большие кружки — атомы кислорода, маленькие кружки — атомы водорода. Прямые линии — связи типа «электронные близнецы», волнистые — типа «дыра и затычка».
Эти цепи называются жирными кислотами, входящими в состав животного жира.
Другие характерные углеродные структуры — это молекулы спиртов, показанные на рис. 35.
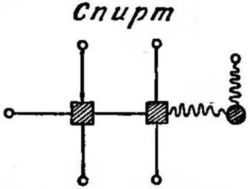
Рис. 35. Молекула спирта C2H5OH. Квадратики — атомы углерода, большие кружки — атомы кислорода, маленькие кружки — атомы водорода; прямые линии — связи типа «электронные близнецы», волнистые — типа «дыра и затычка».
Здесь связи с кислородом образованы по типу «дыры и затычки».
Еще одна важная группа молекул с длинными цепями — это углеводы. Их цепи подобны углеводородным, но к каждому звену цепи присоединен кислород. Он, как всегда, соединяется по типу «дыры и затычки». Простейший углевод — глюкоза, один из видов сахара (рис. 36).
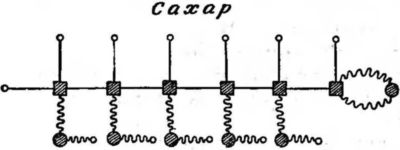
Рис. 36. Сахар. Молекула глюкозы С6Н12О6.
Целлюлоза — также углевод, но с очень длинной цепью. Она встречается в больших количествах в древесине и в других растительных структурах.
Теперь мы переходим к рассмотрению наиболее важной группы молекул — аминокислот, служащих кирпичиками, из которых построена почти вся живая материя. На рис. 37 показан общий принцип построения таких структур.
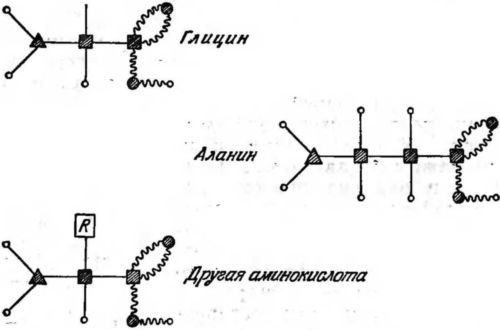
Рис. 37. Аминокислоты. Аминокислоты имеют с одного конца карбоксильную группу, а с другого — аминогруппу NH2. Символом R обозначены химические соединения различного типа.
В скелет этих молекул опять-таки входит углерод с его четырьмя электронными выступами. Наиболее характерны, однако, две их конечные группы. На одном конце молекулы (на рис. 37 справа) находится карбоксильная группа, на другом — аминогруппа NH2. Между двумя конечными группами находится множество других; для каждой аминокислоты характерна ее средняя часть. На рис. 37 показаны две простейшие аминокислоты: глицин и аланин — и общее строение более сложных аминокислот. Две концевые группы аминокислот обладают весьма характерным свойством. Они легко могут соединяться. Аминогруппа и карбоксильная группа связываются друг с другом (так называемая «пептидная связь»), так что аминокислоты легко образуют длинные цепи: одна аминокислота как бы зацепляется за другую. Такие цепи называются белками; как мы узнаем из гл. VIII, они играют важную роль в жизни живых организмов.
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОК