Баллистика и папиросная бумага
Экспериментальные результаты в очередной раз вступили в противоречие с теоретической моделью атома, когда ученик Резерфорда Ханс Гейгер поместил тонкий лист золотой фольги между потоком альфа-частиц и пластиной, регистрирующей частицы. В соответствии с моделью атома, в которой положительный заряд распределен равномерно, как тесто в пудинге, положительно заряженные альфа-частицы, пролетающие сквозь металл, должны испытывать отталкивание со стороны положительного заряда атома. Поскольку заряд распределен равномерно по всему объему атома, значительного отклонения частиц ожидать не приходится.
Гейгер обнаружил, что, вопреки ожиданиям, некоторые альфа-частицы отклонялись в самые разные стороны, вплоть до отражения от золотой фольги непосредственно в том направлении, с которого они прилетели. Резерфорд был ошеломлен: «Это было почти так же невероятно, как если бы вы выстрелили 15-дюймовым снарядом в лист папиросной бумаги, а снаряд вернулся бы назад и попал в вас».
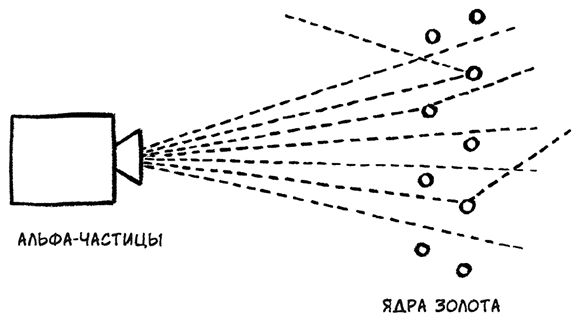
Отклонение альфа-частиц ядрами атомов золота
Новая модель и на этот раз возникла из математических расчетов. Подсчитав, сколько альфа-частиц отклонилось и на какой угол, исследователи обнаружили, что данные соответствуют конфигурации, в которой заряд и масса сосредоточены в малоразмерном объекте в центре атома, который стали называть ядром. Было ли такое ядро неделимым, оставалось неясным.
Когда Резерфорд стал бомбардировать альфа-частицами более легкие атомы, появились свидетельства того, что ядро не является единым объектом, но образовано некими составляющими частицами. Отслеживая траектории альфа-частиц в камере Вильсона, он обнаружил траектории, которые были в 4 раза длиннее, чем ожидалось. Такое могло произойти, если бы попадание альфа-частицы выбивало из ядра другую частицу, в 4 раза более легкую. Эксперименты с разными газами дали одинаковые результаты. Более того, Резерфорд обнаружил, что чистый азот в результате такого столкновения превращается в кислород. Выбивание одной из этих частиц приводило к преобразованию химического элемента.
Так было получено свидетельство существования элементов, из которых построены атомные ядра. Они вели себя в точности как атом водорода, лишенный своего электрона. Резерфорд открыл протон. Атомные ядра оказались построены путем соединения нескольких протонов. Единственное затруднение состояло в том, что электрический заряд не сходился. К примеру, масса ядра гелия в 4 раза больше массы атома водорода, а его заряд больше всего вдвое. Возможно, в ядрах существуют электроны, связанные с протонами и уравновешивающие их заряд. Но физические принципы, которые были разработаны для объяснения поведения этих частиц, исключали столь близкое существование электронов и протонов, так что такой ответ не подходил.
В 1920-х гг. это натолкнуло Резерфорда на догадку о возможном существовании третьей составляющей частицы, названной им нейтроном, имеющей приблизительно ту же массу, что и протон, но не имеющей заряда. Получить свидетельства ее существования оказалось крайне непростой задачей. Резерфорд обсуждал со своим коллегой Джеймсом Чедвиком самые безумные способы, которыми можно было бы обнаружить нейтроны. В конце концов в экспериментах, проведенных в 1930-х гг. в Германии и Франции, были обнаружены частицы, испускаемые при бомбардировке различных ядер альфа-частицами, и частицы эти, в отличие от протонов, по-видимому, не имели заряда. Но экспериментаторы ошибочно считали их каким-то типом электромагнитного излучения наподобие высокочастотных гамма-лучей, которые открыл в начале XX в. французский физик Поль Виллар.
Однако Чедвик был убежден, что эти частицы и есть нейтроны, которые он обсуждал с Резерфордом. Дальнейшие эксперименты показали, что их масса чуть превышает массу протона и именно эта новая частица, не имеющая заряда, оказалась тем ингредиентом, которого недоставало для согласования численных результатов. После открытия Чедвика казалось, что все кирпичики, из которых построена материя, наконец обнаружены.
Модель выглядела чрезвычайно привлекательно. Четыре «стихии» Аристотеля – огонь, земля, воздух и вода – были сведены к трем частицам: электрону, протону и нейтрону. Из этих трех кирпичиков, как считали ученые, можно построить всю материю. Кислород: 8 протонов, 8 нейтронов и 8 электронов. Натрий: 11 протонов, 12 нейтронов и 11 электронов. Как будто бы зазвучала музыка сфер, и в основе материи лежали эти три ноты – протоны, электроны и нейтроны. Вся материя, по-видимому, состояла из целочисленных комбинаций этих трех частиц. Какие были основания ожидать, что и сами эти частицы образованы из еще меньших составляющих? Если бы это было так, то можно было бы рассчитывать увидеть дробные сочетания, расположенные между элементами периодической системы.
Но деление на этом не остановилось. Оказалось, что существуют весьма основательные экспериментальные и математические доводы в пользу делимости протонов и нейтронов. Однако кирпичики, составляющие протоны и нейтроны, обладают одним странным свойством: они не любят находиться в одиночестве. Они встречаются только группами, образуя объекты, подобные протонам или нейтронам. Вместе им безопаснее. Но, если такие частицы никто никогда не видел поодиночке, почему же ученые считают, что такие, еще меньшие, части, на которые можно разделить протоны и нейтроны, существуют?
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОК